|
カルシウム研究のあゆみ 藤田拓男 |
|
はじめに
カルシウムは生体ことに骨格の重要な成分であり、さらに細胞の情報伝達に不可欠な元素である。生命の源として数十億年の生命の歴史とともに常にあらゆる生体の中に存在していたはずであるが、実際にカルシウムが発見されたのは、比較的新しく19世紀初頭である。
、地表には石灰岩がいろいろな所に存在しており、ラテン語の石灰Calxから、新しく発見された元素はカルシウムと名づけられた。
、地殻の3%はカルシウムで占められており、アルミニウムとともに最も多く含まれる元素である。化石は約30億年の歴史をもち、生命の地上に残した足跡であるが、地殻に含まれているカルシウムもその起源は太古の海の中の生物の内外骨格など、生体に関連のあるものであり、生命がカルシウムとともにはじまり、カルシウムが生命を支えてきた歴史を物語るものである。
生体が常に栄養を摂取し、自らを更新していくことが生存のために必要な以上、体成分をすべて栄養成分として常に摂取していくことは必要であり、この意味でカルシウムが栄養成分の一つとして必要なことは疑う余地はない。
、また、情報伝達のうえでのカルシウムの重要性からみて、その体内各分画、細胞内外での精密なコントロールが要求される点、カルシウムはほかの多くの体成分に比してユニークであるといえる(*1)。
1.元素としてのカルシウムの発見とその生理的意義の解明
1808年6月、Humphry Davy (*2)はロンドンの研究所で、石灰と酸化水銀の混合液に自分のつくった大きな電池で通電してアマルガムをつくり、蒸留して水銀を除いた後に、少量の銀色に輝く灰白色粉末としてはじめてカルシウムを分離した。
細胞の基本的な機能である情報伝達に、カルシウムが不可欠であることをはじめて認めたのは Sidney Ringer であった。カルシウムは地表にあまりにも多く存在するので、その発見に至る経路は共存する不純物や妨害物質を取り除き、前からそこにあったカルシウムを確実に認識できるようになった過程であるともいえる。
Ringer (*3)がカルシウムの心収縮における重要な役割を発見したのも劇的ともいえる幸運に基づくものであった。ロンドンの水道水に大量のカルシウムの含まれていることを知らなかった Ringer は、蛙の心臓を持続して収縮させるには生理的濃度の食塩水で十分であると考えていた。実験助手の怠慢から水道水に食塩を加えて使っていた Ringer は、ある日自分で蒸留水をつくりこれに食塩を加えて蛙の心臓が動かないことを知って驚いた。ロンドンの水道水の中の心臓の収縮を支える未知の物質、これがカルシウムであった。
、Heibrun により細胞の生命にカルシウムが不可欠であることがその後次第に明らかとなった。
2.栄養物としてのカルシウムの摂取とその歴史的変遷
約 2億年前に哺乳類がはじめて地上に出現してから1億5千年ぐらいの間、昆虫がその主な食物であった(*4)。昆虫体のカルシウムの含量は124mg/100gであって獣肉より高い。またその後の混合食の時代になって木の葉、果物なども食べるようになってからも、カルシウムの摂取は現代人のそれよりもはるかに高く2倍以上であり、石器時代にまでこの傾向は続いたと考えられる(*6)。
、食塩や脂肪の摂取量は、はるかに現代より低いと考えられるので、食物繊維の量は多少多かったとしても、吸収され利用されるカルシウムの量は現代よりはるかに大きいものであったと思われる。
、蛋白やリンの摂取量もおそらく現代人のそれより多かったと思われるが、カゼインやグルテンのような精製された蛋白の摂取が尿中カルシウムの排泄を増加させるのと異なり(*7)、肉食中心の1日2gのカルシウム摂取でもカルシウムの喪失は少なかったとの報告もある。
、運動量やほかの生活全般にわたる諸因子の影響を考えなければカルシウム摂取量の適否の判定は困難であろう。
、このような狩猟生活を中心とした原始人類は身長も高かったが、約1万年ぐらい前から農耕に従事することが多くなり、カルシウム含量が少なく、また吸収され難い穀物を主食とするようになって身長も短縮の傾向を示した。カルシウムの摂取量が身長の大きな決定因子であることは、戦後の日本人の急速な身長の伸びからみても理解しやすいことである。
、骨粗鬆症の発生についても、カルシウム摂取の多かったと思われる狩猟時代には少なかったと思われる。農耕時代よりも骨量は安定していて加齢による減少が少なかったといわれる(*8)。
現在の人類の中にも比較的カルシウム摂取の多い西欧の先進工業国と、これよりはるかに少ない農耕に主として従事する発展途上国があり、身長も一般に西欧人の方が高いのは興味あることである。
3.カルシウムの体内分布とその生理的役割
カルシウムは体内で5番目に多い元素であり、有機物をつくる炭素・水素・酸素・窒素に次いで、無機物の中で最も多く、その99%は骨にある。すなわちカルシウムは人体の構成分として不可欠なものであるから、その一定量の摂取が人体の成分を一定に保つうえに重要であることはいうまでもない。しかしながら、これにも増して重要なカルシウムの役割は、細胞の情報伝達を担っていることにある。このために、カルシウムは、体内で他に類をみない独特の分布を示す(図1)。 すなわち、最も精密に維持されている生物学的恒数としての血清あるいは細胞外液中のカルシウムイオン濃度は約1mMであり、カルシウム摂取量・排泄量の変動があってもその変化の幅はきわめて小さく、一定の値に保たれている。これは、その10,000倍の巨大なカルシウムのプールである骨から、カルシウム調節ホルモンの働きによって必要な量が出納されるためである。 |
【図1】体内のカルシウム分布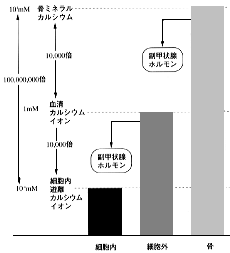 |
血清カルシウムを一定に保たなければならない理由の一つはその10,000分の1しかないきわめて低い細胞内遊離カルシウムイオン濃度と平衡を保つためである。細胞膜の最も重要な役割は、細胞の内外の環境をはっきりと区別すること、すなわち細胞内のカルシウムの真空状態ともいえる低い濃度を、きわめて高い細胞外液の濃度に対して一定に保つことにある。
このために細胞膜はカルシウム関門を備えて、必要な場合だけカルシウムに対して門を開く。
、一方細胞内のカルシウムは、カルシウムポンプで絶えず外に汲み出す。細胞の中にもいくつかの小器官(小胞体・ミトコンドリア等)があって、その中には細胞外液に近い濃度のカルシウムが含まれており、したがって小胞体などの膜も細胞膜と同様に細胞質内遊離カルシウムイオンを増加させないようにする役割をもつ。相接するコンパートメントの間の大きなカルシウム濃度の落差とこれに伴う緊張がカルシウムによる情報伝達の鍵であるといえる。
したがってカルシウムの役割は、1)骨に十分な量が存在して支持組織としての骨に強度を与えること、2)体内における特殊な分布によって細胞の情報伝達を保証し、その機能を助けることである(*9,10)。
カルシウムの摂取の不足は、体内のカルシウム貯蔵量およびその分布にどのような影響を蛋白質与えるであろうか。消化液および尿中へのカルシウムの排泄は摂取量にかかわらず常に一定量が起こっているので( obligatory loss )、もしも摂取量が少なければ血清カルシウムが低下することになる。
、副甲状腺細胞にはカルシウムセンサー(受容体)があり、わずかの血清カルシウムの低下もこれを感知して副甲状腺ホルモンの分泌を起こす(*11)。副甲状腺ホルモンは骨芽細胞を介して破骨細胞性骨吸収を亢進させ、骨のカルシウムを血液へ動員して血清カルシウムを上昇させもとにもどす。
、すなわち図1に示すように、副甲状腺ホルモンは骨ミネラルのコンパートメントから、細胞外液のコンパートメントへカルシウムを移動させ、両者の間の落差を軽減させる。細胞内外のコンパートメントでも、副甲状腺ホルモンは同じ方向に働く。すなわち、細胞の外から中へカルシウムイオンを押し込む傾向があり、L型のカルシウム関門を活性化することによってこのような作用を示すことが、標的細胞としての骨芽細胞や腎尿細管細胞のほかに、心筋細胞、リンパ球、白血球、血管平滑筋細胞、脂肪細胞、膵ラ氏島β細胞等で認められる。
、一時的な細胞内遊離カルシウムイオンの増加は、細胞機能の発現のために必要なことではあるが、常に副甲状腺ホルモンが働いて同様のことが繰り返されると、細胞内遊離カルシウムの基礎値が上昇して細胞外のカルシウムのレベルとの落差が小さくなり、細胞内遊離カルシウムの増加が増加として認識されなくなる。このことは、その細胞の情報伝達に重大な障害が起こることを意味する。
個体レベルではカルシウムの摂取がいつも不足していると副甲状腺ホルモンの分泌が絶えず起こり、骨のカルシウム含量は減少し、また血管や軟骨などの関節周囲組織、脳その他の神経組織などのいわゆる軟部組織、すなわち通常はカルシウムをほとんど含まない組織でのカルシウム含量が増加する。軟部組織だけをみているとカルシウムの摂取過剰の結果ではないかと思われるが、実はカルシウムが不足しているために、副甲状腺ホルモンの分泌が増加して骨からカルシウムが動員された結果であって、逆説的であるから、カルシウム・パラドックスといわれる。
、心筋の灌流で、カルシウムを含まない液を用いた後にカルシウムを含む液で灌流すると、心筋細胞内でカルシウムが急激に増加して細胞障害が起こることがカルシウム・パラドックスとしてはじめて記載された(*12)。これと全身レベルでの老化のカルシウム・パラドックスは、カルシウム欠乏のあとにカルシウム過剰とその障害作用が起こるという共通のパターンがある。
4.カルシウムと骨粗鬆症
カルシウムの不足が骨粗鬆症を起こしうるということが指摘されたのはあまり古いことではない。Nordin (*13,14)がビタミンD欠乏によって血清カルシウムXリン積が低下して起こる石灰化不全すなわち骨軟化症またはくる病と、カルシウムだけの不足でビタミンDの必要はほぼ満たされているので、血清生化学所見は正常であるが、骨量の減少する骨粗鬆症とを区別したのは1960年ごろであった。それまで Albright のエストロゲン欠乏による閉経後骨粗鬆症の考え方が1947年ごろから支配的で、Nordin の説は受け入れられる前にさらに長い時間を必要とした。
最もよく引用される報告は、Matkovic らのユーゴスラビアのカルシウム摂取量の、明らかに異なる2つの地域における骨量と骨折頻度の比較である。これらの2つの地域はカルシウム摂取だけでなくほかの栄養摂取や生活習慣も異なり、骨粗鬆症の差をカルシウムだけで説明できるか否かは異論もあるが、明らかにカルシウム不足が骨粗鬆症の発生を促進する可能性を示した最初の報告であった。
カルシウムの欠乏が骨粗鬆症の原因またはその病態生理に重要であるか否かについては、現在までにいろいろな意見があり、必ずしも一致をみていない(表1)。
| 【表1】カルシウムが骨粗鬆症に重要であるかないかについての議論 | |
| 重要である | 重要でない |
| 骨粗鬆症(脊椎圧迫骨折)のある人はカルシウム摂取が少ない Nordin (*13,14) | カルシウム摂取の低いアジアで、カルシウム摂取の高い北欧より大腿頸部骨折が少ない Kanis (*16) |
| ユーゴスラビアの低カルシウム摂取地域の人は高カルシウム摂取地域の人より骨量が低く骨折が多い Matkovic (*16) | 閉経後の骨量減少にはカルシウムよりもエストロゲンの方がより有効である Riis (*17) |
| 37のカルシウム補給についての論文を評価し高いカルシウムの摂取が閉経後の骨量減少を予防することを認めた Cumming (*18) | 閉経後の骨減少はカルシウム摂取と相関しない Riggs (*19) |
| 老人の骨粗鬆症ではビタミンDとカルシウムの補給によって骨折の頻度を減少させることができる Meunier (*20) | カルシウム摂取は高いレベルでも低いレベルでも適応機序があり一定の閾値を越える摂取は無効である Nilas (*21) |
その主な理由としては、
、1)カルシウム摂取は世界各国、各地域で大きく異なるが、これが必ずしも骨粗鬆症の発生率や合併症としての頻度と相関を示さない。骨粗鬆症は栄養のほかに遺伝、運動等の生活習慣とも関係の深い多因子疾患であることから理解しうる。
、2)骨粗鬆症は女性に多く、閉経後にエストロゲン分泌の停止とともに急速な骨減少が起こり、これを防止するうえにはエストロゲンが最も有効である。
、3)カルシウムを補充するとき、現在までに用いられているカルシウム製品の腸管からの吸収は低いものであり、十分に吸収され利用されているとはいえない。このことが、カルシウム補給による骨粗鬆症の改善効果を不十分なものにしている。非常に吸収のすぐれたカルシウムであれば、現在までのカルシウムについての常識を打ち破るかもしれない。
| 【図2】骨粗鬆症の予防におけるカルシウムの重要性と 他の因子との関連(骨づくりの3条件) 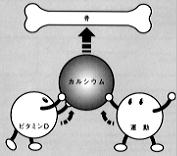 |
、また、カルシウムの吸収・利用にはビタミンDその他の栄養因子と運動などが吸収を促進するので、独立した因子ではない(図2)。 ■・項目に戻る |
5.カルシウムの所要量、必要量、目標量
カルシウムの必要量についても多くの混乱がある。必要量の出発点は代謝出納に基づいており、どのような場合でも必ず失われるカルシウムの量(不可避損失)を補うのにどれだけのカルシウムの量が必要かという計算に基づいており、したがって各人で異なり、厳密に必要量を求めるには一人一人で出納試験を行わなければならない。
、そこで、平均的な人の必要量を推定し、これに約10〜20%の安全域を加えたものが所要量であり、日本人では成人は1日600mg、欧米では多く800mgくらいである。しかしながら成長や妊娠、加齢に伴ってカルシウムの必要量と腸管吸収は変化し、ことに閉経後は加齢とともに腸管からのカルシウムの吸収が低下するので、これを補うためにはさらに多くのカルシウムを摂ることが望ましいとされる。
、NIHで行われた専門家の会議では、閉経後女性では1日1,500mgが望ましいとされ(*22)、また Michaelsson もスウェーデンで1,500mg以上のカルシウムをとらなければ骨量維持の効果が認められないとしている(*23)。
、Riggs らは加齢によるカルシウム欠乏のための血中副甲状腺ホルモンの上昇は、1日2,400mgのクエン酸カルシウムをとってはじめて正常化したと述べている。すなわち必要ぎりぎりの所要量に比べて、高齢でも健康を保つための目標量はかなり高いものであろうと考えられる(*24)。
6.カルシウムと健康
カルシウムの不足にもかかわらず、血清カルシウムを維持するために、副甲状腺ホルモンが分泌されて骨からカルシウムをとりだし、軟部組織や細胞内の本来カルシウムの少ない所でのカルシウム濃度を増加させ、この傾向が加齢とともに強くなって老化の続発性副甲状腺機能亢進症を起こす。
、骨のカルシウムの減少する骨粗鬆症のほかに、高血圧、動脈硬化、老人性痴呆、糖尿病、免疫異常、悪性腫瘍等、加齢に伴って増加する多くの疾患の背景となる。このために単に所要量を充たすだけでなく、より高い目標を設置して加齢に伴う続発性副甲状腺機能亢進症を主としたカルシウム代謝の異常を改善することは、多くの成人病−生活習慣病の予防と治療につながる。
人の病気は細胞の病気であり、すべての細胞の病気は細胞内カルシウムの増加を最終共通経路とする以上、生活習慣病はカルシウム欠乏症であり、十分なカルシウムの摂取は健康と長寿への道であるといえる。
| 【図3】カルシウム・パラドックスとカルシウム欠乏症 | ||||||||||||||||||||||||||||||||||
| カルシウム不足 ↓ 副甲状腺ホルモン分泌亢進 ↓ 細胞内カルシウム増加 ↓ 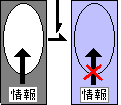 |
━ |
| ||||||||||||||||||||||||||||||||
参考文献
| (*1) | Campbell AK : The natural history of calcium. Intracellular Calcium Its Universal Role as Regulator. John Wiley & Sons, pp2-22,1983 |
| (*2) | Davy H : Electrochemical researches on the decomposition of the earths with observation on the metals obtained from alkaline earths and on the amalgam from |
| (*3) | Ringer S : Concerning the influence exerted by each of the constituents of blood on the contraction of the ventricle. J Physiol3:380-393,1882 |
| (*4) | Eaton SB, Nelson DA : Calcium in evolutionary prospective. Amer Clin Nutr 54:281 S-287 S.1991 |
| (*5) | Eaton SB, Konner MJ : Paleolithic nutrition : a consideration of its nature and current implications. N Engl Med 312:283-289,1985 |
| (*6) | Johnson NE, Alcantara EN, Linkswilew H : Effect of level of protein intake on urinary and fecal calcium retention of young adult males. J Nutr 100:1425-1430,1970 |
| (*7) | Spencer H, Kramer L, Debartolo M, Norris C, Osis D : Further studies on the effect of high protein diet as meat on calcium metabolism. Am J Clin Nutr 37:924-929,1983 |
| (*8) | perzigian AI : Osteoporotic bone loss in two prehistoric Indian populations. Am J Phys Anthropol 39:87-95,1973 |
| (*9) | Fujita T : Aging and calcium. Miner Electrolo Metab 12:149-156,1986 |
| (*10) | 藤田拓男:副甲状腺。日本内科学会雑誌 79:23-31,1990 |
| (*11) | chattopadhyay N, Mithal A, Brown EM : The calcium-sensing receptor.A window into the physiology and pathophysioloy of mineral ion metabolism. Endocr Rev 17:289-307,1996 |
| (*12) | Goshima K, Wakabayashi S, Masuda A : Ionic mechanism of morphological changes in cultured myocardial cells on successive incubation in media without and with Ca++. J Mol Cel Cardiol 12:1135-1157,1980 |
| (*13) | Nordin BEC, Marshall DH : Dietaly requirement for calcium in Human Life (Nordin BEC,ED)Springer verlag, Berlin pp447-471,199 |
| (*14) | Nordin BEC : Clinical significance and pathogenesis of osteoporosis. Brit Med J 1:571-576,1971 |
| (*15) | Matkovic V, Kostial K, Simonovic I, Buzina R, Bradarec I, Nordin BEC : Bone status and fractue rates in two regions of Yugoslavia. am J Nutr 32:540-549,1979 |
| (*16) | Kanis JA, Passmore R : Calcium supplementation of the diet. Not justified by present evidence. Brit Med J 298:137-140,1989 |
| (*17) | Riis B, ThomsenK, Christiansen C : Does calcium supplementation prevent postmenopausal bone loss? N Engl JMed 316:173-177,1987 |
| (*18) | Cumming RG : Calcium intake and bone mass ; Aquantitative review of evidence. calcif Tissue Int 47:194-201,1990 |
| (*19) | Riggs BL, Wahner HW, Melton LJ lll, Richelson LS, Judd HL, O'Fallon WM : Dietary calcium intake and rates of bone loss in woman. J Clin Invest 80:979-982,1987 |
| (*20) | Meunier PJ, Chapuy MC, Arlot ME, Delmas PD, Duboeuf F : Can we stop bone loss and prevent hip fracture in the elderly? Osteopor Int 1:S71-76,1994 |
| (*21) | Nilas L : calcium intake and osteoporosis. Smopoulos AP, GaIIC(eds) Osteoporosis : Nutritional Aspects, Kargar pp 1-26,1993 |
| (*22) | Optimal calcium intake Nutrition 11:409-417,1995 |
| (*23) | Michaelsson K, Holmberg L, Sorensen S, Wolk A, Bergstrom R, Ljunghall S : Diet and hip fracture risk. A case controled study. Int Epidemiol 24:771-782,1995 |
| (*24) | Riggs BL, O' Fallon WM, Muhs J, O'Connor MK, Melton LJ lll : Long term effects of calcium supplementation on serum PTH, bone turnover and bone loss in eldely women. J Bone Mener Res 11:Suppl 1:S118,1996 |